ขนาด อะตอม ตาราง ธาตุ
2445 เฮนรี กวิน เจฟฟรีส์โมสลีย์พบว่า ตารางธาตุต้องเรียงตามเลขอะตอม หรือจำนวนโปรตอน จะสอดคล้องกับกฎพีริออดิก โดยไม่ต้องสลับที่กันเหมือนกับการเรียงมวลอะตอม การเรียกชื่อธาตุที่มีเลขอะตอม 100 ขึ้นไป ตามระบบ IUPAC (International Union of Pure and Applied Chemistry) . ใช้เลขเป็นภาษาละตินลงท้ายด้วย -ium ถ้าสระซ้ำ 2 ตัวให้ตัดออกก 1 ตัว เช่น bi + iumเป็น biumและ tri + iumเป็น trium ถ้าพยัญชนะซ้ำ 3 ตัว ให้ตัดออก1 ตัว เช่น enn + nil เป็น ennil 1. การรับจ่ายอิเล็กตรอนและโปรตอน การรับจ่ายอิเล็กตรอน จะทำให้ธาตุอยู่ในรูปของไอออน การรับจ่ายโปรตอน ธาตุจะเปลี่ยนไปจากธาตุเดิม 2. การจัดเรียงอิเล็กตรอนเหมือนแก๊สเฉื่อย คือธาตุต่อไปนี้ ธาตุหมู่ I เป็นไอออน +1 ธาตุหมู่ IIที่เป็นไอออน +3 ธาตุหมู่ IIIเป็นไอออน +3 ธาตุหมู่ IVเป็นไอออน -1, +1 ธาตุหมู่ Vเป็นไอออน -3, +5 ธาตุหมู่ VI เป็นไอออน -2, +6 ธาตุหมู่ VIIเป็นไอออน -1, +7 3. สมบัติของค่าต่างๆ ในตารางธาตุ 3. 1 ขนาดอะตอม (รัศมีอะตอม) การบอกขนาดจะบอกเป็นค่าของรัศมีอะตอม ตามหมู่ ขนาดอะตอมจะโตขึ้น ถ้าเลขอะตอมเพิ่มขึ้น (บนลงล่าง) เพราะระดับพลังงานเพิ่มขึ้น ตามคาบ ขนาดจะเล็กลง ถ้าเลขอะตอมเพิ่มขึ้น (ซ้ายไปขวา) เพราะธาตุแต่ละตัวอยู่ในระดับพลังงานเดียวกัน แต่จำนวนโปรตอนเพิ่มมากขึ้น จึงดึงดูดอิเล็กตรอนให้เล็กลง 3.
- ตารางธาตุ ใช้หลักเกณฑ์อะไรสำหรับการจัดเรียงธาตุแต่ละชนิดลงในตาราง
- ขนาดอะตอมของธาตุ - ตารางธาตุ
- ตารางธาตุ | โครงสร้างอะตอม และ ตารางธาตุ
- ตารางธาตุพร้อมชื่อและน้ำหนักอะตอมใหญ่ - วิกิพีเดีย
- ขนาดอะตอม ตารางธาตุ
ตารางธาตุ ใช้หลักเกณฑ์อะไรสำหรับการจัดเรียงธาตุแต่ละชนิดลงในตาราง
- ตารางธาตุ ใช้หลักเกณฑ์อะไรสำหรับการจัดเรียงธาตุแต่ละชนิดลงในตาราง
- Soul korea town เอกมัย cast
- ตารางธาตุ | โครงสร้างอะตอม และ ตารางธาตุ
- เว็บ ตัด ต่อ
- ขนาดอะตอมของธาตุ - ตารางธาตุ
- แปล เพลง 24 7 free
- วัด บัว ผัน บางขุนเทียน จังหวัด
- กรวย จราจร ขนาด มาตรฐาน
80(1) รูบิเดียม 37 Rb 85. 4678(3) สตรอนเชียม 38 Sr 87. 62(1) อิตเทรียม 39 Y 88. 90585(2) เซอร์โคเนียม 40 Zr 91. 224(2) ไนโอเบียม 41 Nb 92. 90638(2) โมลิบดีนัม 42 Mo 95. 94(1) เทคนีเตียม 43 Tc [97. 9072] ลูทีเตียม 44 Ru 101. 07(2) โรเดียม 45 Rh 102. 90550(2) แพลเลเดียม 46 Pd 106. 42(1) เงิน 47 Ag 107. 8682(2) แคดเมียม 48 Cd 112. 411(8) อินเดียม 49 In 114. 818(3) ดีบุก 50 Sn 118. 710(7) พลวง 51 Sb 121. 760(1) เทลลูเรียม 52 Te 127. 60(3) ไอโอดีน 53 I 126. 90447(3) ซีนอน 54 Xe 131. 29(2) ซีเซียม 55 Cs 132. 90545(2) แบเรียม 56 Ba 137. 327(7) 57-71 * แฮฟเนียม 72 Hf 178. 49(2) แทนทาลัม 73 Ta 180. 9479(1) ทังสเตน 74 W 183. 84(1) รีเนียม 75 Re 186. 207(1) ออสเมียม 76 Os 190. 23(3) อิริเดียม 77 Ir 192. 217(3) ทองคำขาว 78 Pt 195. 078(2) ทองคำ 79 Au 196. 96655(2) ปรอท 80 Hg 200. 59(2) แทลเลียม 81 Tl 204. 3833(2) ตะกั่ว 82 Pb 207. 2(1) บิสมัท 83 Bi 208. 98038(2) พอโลเนียม 84 Po [208. 9824] แอสทาทีน 85 At [209. 9871] เรดอน 86 Rn [222. 0176] แฟรนเซียม 87 Fr [223. 0197] เรเดียม 88 Ra [226. 0254] 89-103 ** รัทเทอร์ฟอร์เดียม 104 Rf [263.
ขนาดอะตอมของธาตุ - ตารางธาตุ

ขนาดอะตอมของธาตุ หน่วยพิโกเมตร ขนาดอะตอมของธาตุต่างๆ ขนาดของอะตอมนั้นถ้าจะพิจารณาถึงปัจจัยต่างๆ ที่ส่งผลกระทบต่อขนาดของอะตอมนั้น อาจแบ่งแยกออกได้เป็นข้อ เรียงตามลำดับความสำคัญได้ดังนี้ 1. จำนวนระดับพลังงาน 2. จำนวนโปรตอน 3. จำนวนอิเล็กตรอน
ตารางธาตุ | โครงสร้างอะตอม และ ตารางธาตุ
– เรื่องอื่นๆ ที่น่าสนใจ: ธาตุและสารประกอบ (Elements and Compounds)

ตารางธาตุพร้อมชื่อและน้ำหนักอะตอมใหญ่ - วิกิพีเดีย
เนื้อหา 1. วิวัฒนาการของตารางธาตุ 2. สมบัติทั่วไปของตารางธาตุ 3. เลขออกซิเดชัน 4. สมบัติของสารประกอบของธาตุตามคาบ 5. สมบัติของธาตุแต่ละหมู่ 6. ตำแหน่ง H ในตารางธาตุ 7. สมบัติของธาตุแทรนซิชัน 8. สมบัติของสารประกอบของธาตุแทรนซิชัน พ. ศ. 2360 โยฮันน์เดอเบออไรเนอร์ได้จัดธ่าตุเป็นกลุ่มที่มีลักษณะคล้ายกัน เรียกว่า ชุดสาม เช่น Na จะมีมวลอะตอมเป็นค่าเฉลี่ยของธาตุ Li กับ K เป็นต้น พ. 2407 จอห์น นิวแลนส์อเล็กซานเดอรส์ รีนา เสนอว่า ถ้านำธาตุมาเรียงลำดับตาม มวลอะตอม จะพบว่าธาตุที่8 จะมีสมบัติคล้ายกับธาตุหมู่ที่ 1 (ไม่รวม H กับแก๊สเฉื่อย) Li Be B C N O F Na Mg Al Si P S Cl K Ca พ. 2412 – 2413 ยูลิอุสโลทาร์ ไมเออร์ และ ดิมิทรี อิวาโนวิช เมนเดเลเอฟ จัดเรียงตารางธาตุตาม มวลอะตอม พบว่า ธาตุมีสมบัติที่คล้ายคลึงกันเป็นช่วงๆ จากคุณสมบัติของธาตุที่มีความคล้ายคลึงกันนี้เอง เมนเดเลเอฟจึงตั้งกฎขึ้นมา ชื่อว่า "กฎพีริออดิก" การจัดเรียงธาตุของเมเดเลเอฟ จึงไม่ได้ยึดการจัดเรียงลำดับแค่มวลอะตอม จากน้อยไปมากเท่านั้น แต่ยังยึดหลักการของ "กฎพีริออดิก" คือ ธาตุที่นำมาจัดเรียงในกลุ่มเดียวกันต้องมีคุณสมบัติคล้ายคลึงกัน พ.
ตารางธาตุ เป็นอีกหนึ่งเครื่องมือของนักเคมีที่ช่วยจัดระเบียบของธาตุต่าง ๆ ที่ค้นพบ ทำให้เราจำสมบัติของธาตุได้ง่ายเนื่องจากสมบัติเหล่านั้นของธาตุในตารางธาตุมีแนวโน้มอย่างชัดเจน ดังนั้นถ้าเราทราบสมบัติของธาตุหนึ่ง เราก็สามารถทำนายสมบัติของธาตุอื่นได้ด้วย เช่น เราทราบว่าขนาดอะตอมของ Li เท่ากับ 152 พิโคเมตร แล้วขนาดอะตอมของ Be เป็นเท่าใด เราสามารถตอบอย่างคร่าว ๆ ว่า "ควรจะมีขนาดอะตอมน้อยกว่า 152 พิโคเมตร" เป็นต้น สมบัติของอะตอมตามตารางธาตุ ได้แก่ 1. ขนาดอะตอม (atomic size) 2. พลังงานไอออไนเซชัน (ionization energy; IE) 3. สัมพรรคภาพอิเล็กตรอน (electron affinity; EA) 4. อิเล็กโทรเนกาติวิตี (electronegativity; EN) ขนาดอะตอม (atomic size) ความหมาย ขนาดของอะตอม วัดจากระยะห่างระหว่างนิวเคลียสของอะตอมที่อยู่ติดกัน สำหรับธาตุที่อยู่ในลักษณะโมเลกุลอะตอมคู่ รัศมีอะตอมจะถือว่าเป็นครึ่งหนึ่งของระยะระหว่างนิวเคลียสของ 2 อะตอมในโมเลกุล จากรูป ระยะห่างระหว่างอะตอมของคลอรีนเท่ากับ 99 พิโคเมตร ส่วนคาร์บอนเท่ากับ 77 พิโคเมตร แนวโน้มขนาดอะตอมของธาตุต่าง ๆ ในตารางธาตุ ปัจจัยที่มีผลต่อขนาดอะตอม 1. เลขควอนตัมหลัก(n)ของเวเลนซ์อิเล็กตรอน 2.
ขนาดอะตอม ตารางธาตุ
เปรียบเทียบขนาดอะตอมของไอโอดีนกับโลหะและอะลูมิเนียมอะลูมิเนียมอะลูมิเนียมอะลูมิเนียมอะลูมิเนียมอะลูมิเนียมอะลูมิเนียมอะลูมิเนียม ลดลงด้วยสมมติฐานที่ว่าได้แรงดึงดูดระหว่างประจุไฟฟ้าในห้างหุ้นส่วนจำกัดนิวเคลียสกับคุณอิเพิ่มข้อมูลที่ทรอนิคส์จะเพิ่มมากขึ้น ะตอมอะลูมิเนียมเป็นส่วนคุณหนึ่งของอะลูมิเนียมที่มีขนาดใหญ่และมี กำลังการผลิตสูงขึ้นเรื่อย ๆ ขยายออกไปจากที่เดิมไอโอเนตดั งนั้นจึงมีขนาดใหญ่กว่าอะตอม มิวสิกวิดีโอตัวอย่างขนาดอะนิเมะกับขนาดของไอโอดีน 12. รัศมีอะนิเมชั่นและรัศมีไอโอโนเมียและไอเรียลมีแนวโน้มที่จะเป็นเหมือนอะตอมและไอโอ โนเบลไอโอดีน แต่รัศมีไอโอซอนมีค่า คล้ายคลึงกันหรือ มีลักษณะคล้ายคลึงกันหรือมีลักษณะคล้ายคลึงกันหรือมีลักษณะคล้ายคลึงกันหรือมีลักษณะคล้ายคลึงกัน จะมีขนาดเล็กกว่าไอโอดีน 3+ จะมีขนาดเล็กกว่า 2+ และ 1+ ตามลำดับ 13. ความหมาย 14. พลังงานไอออไนเซชัน คือ พลังงานที่ใช้ในการดึงอิเล็กตรอน 1 อนุภาค ออกจากอะตอมในสถานะแก๊ส กลายเป็นไอออนบวก 15. 815 กิโลจูล / โมลจากการสังเกตจากค่าพลังงานไอออไนเซชันจะพบว่า IE1 คือพลังงานที่ให้แก่อะตอมเพื่อดึงอิเล็กตรอนที่อยู่วงนอกสุด (เวเลนซ์อิเล็กตรอน) มีค่าน้อยที่สุดเพราะอิเล็กตรอนที่อยู่ห่างจากนิวเคลียสหลุดออก ได้ง่ายไม่ต้องใช้พลังงานมากเพราะได้รับแรงดึงดูดจากนิวเคลียสน้อย แต่อิเล็กตรอนที่อยู่ใกล้นิวเคลียสจะถูกดึงดูดไว้เราต้องใช้พลังงานมากเพื่อที่จะทำให้อิเ ็กตรอนนั้นหลุดออกมาดังนั้นค่า IE3 จึงมีค่ามากที่สุด 16.
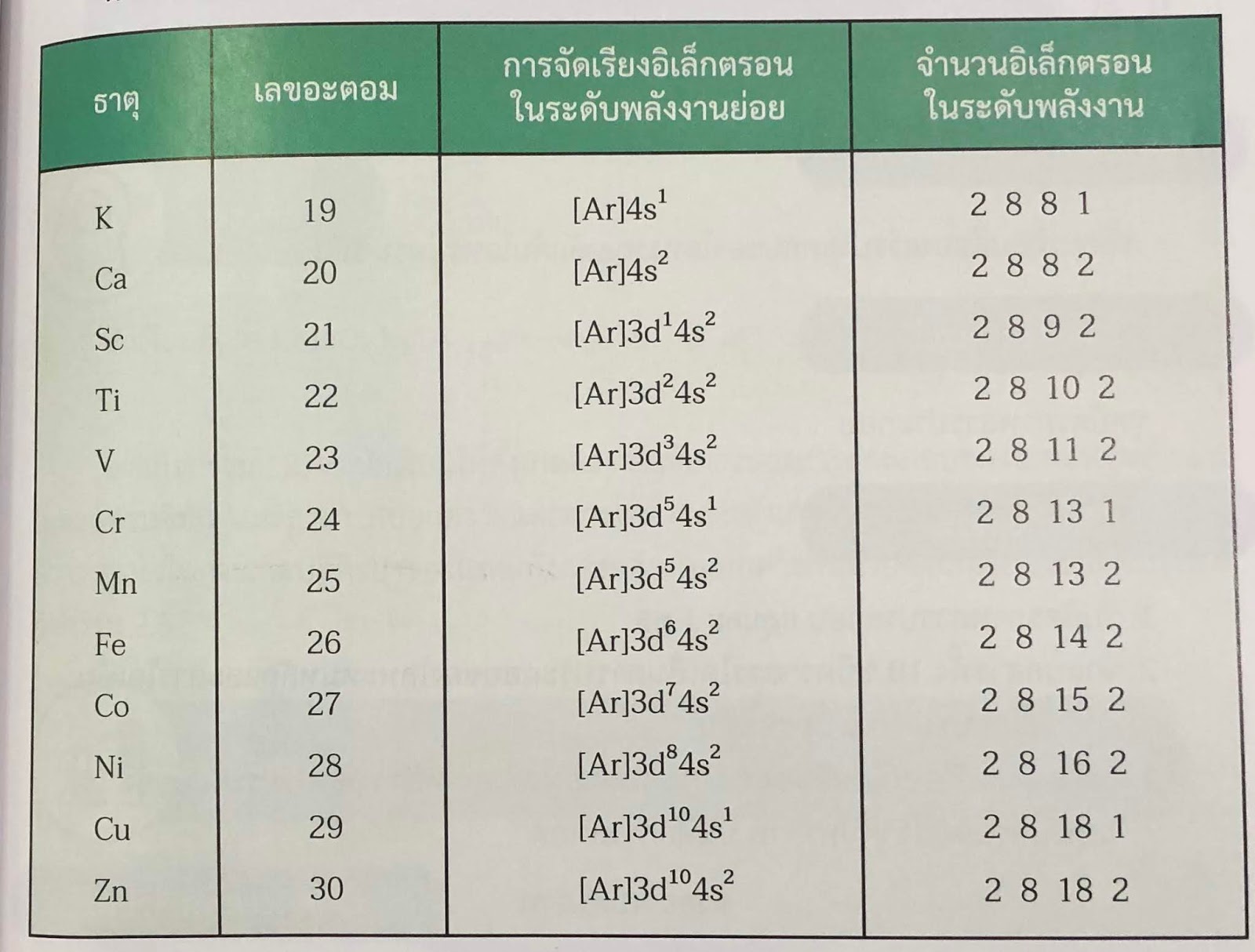
3 จงเรียงอิเล็กตรอนของธาตุและไอออนต่อไปนี้ 7. 4 ธาตุ Transition จะมีเวเลนต์อิเล็กตรอนเป็น 2, 1เท่านั้น Cr กับ Cu มีเวลนซ์อิเล็กตรอน เท่ากับ 1 7. 5 ธาตุ Transition จะมีสมบัติเหมือนกันเป็นคาบมากกว่าเป็นหมู่ 7. 6 ความหนาแน่นของธาตุ Transition จะสูงมาก และสูงอยากใกล้เคียงกันมากในคาบเดียวกัน 7. 7 จุดเดือด จุดหลอมเหลว ของธาตุ Transition จะสูงมาก 7. 8 ค่า IE, EN ของธาตุ Transition จะสูงมากกว่าโลหะโดยทั่วไป 7. 9 ขนาดอะตอมเรียงตามคาบจะเล็กลง แต่ใกล้เคียงมาก เพราะ Transition มีความหนาแน่นสูง 7. 10 ธาตุ Transition มีเลขออกซิเดชันหลายค่า ยกเว้น Scกับ Zn มีเลขออกซิเดชัน ค่าเดียว ตรงกลางของคาบจะมีจำนวนเลขออกซิเดชันมาก และมีค่าสูง ส่วนปลายทั้งสองจะมีค่าลดลง เช่น 8. 1 เกิดสี 8. 2 เกิดสารประกอบเชิงซ้อน (Complex) เกิดสี ของสารประกอบของธาตุ Transition การเกิดสารประกอบเชิงซ้อน ไอออนเชิงซ้อน คือ ไอออนที่มีธาตุตั้งแต่ 2 ชนิดขึ้นไปเป็นองค์ประกอบ เช่น